ELECTRON
Elektron adalah partikel subatom yang bermuatan negatif dan umumnya ditulis sebagai e-. Elektron tidak memiliki komponen dasar ataupun substruktur apapun yang diketahui, sehingga ia dipercayai sebagai partikel elementer.[2] Elektron memiliki massa sekitar 1/1836 massa proton.[3] Momentum sudut (spin) instrinsik elektron adalah setengah nilai integer dalam satuan ħ, yang berarti bahwa ia termasuk fermion. Antipartikel elektron disebut sebagai positron, yang identik dengan elektron, tapi bermuatan positif. Ketika sebuah elektron bertumbukan dengan positron, keduanya kemungkinan dapat saling berhambur ataupun musnah total, menghasilan sepasang (atau lebih) foton sinar gama.
Elektron, yang termasuk ke dalam generasi keluarga partikel lepton pertama,[4] berpartisipasi dalam interaksi gravitasi, interaksi elektromagnetik dan interaksi lemah.[5] Sama seperti semua materi, elektron memiliki sifat bak partikel maupun bak gelombang (dualitas gelombang-partikel), sehingga ia dapat bertumbukan dengan partikel lain dan berdifraksi seperti cahaya. Oleh karena elektron termasuk fermion, dua elektron berbeda tidak dapat menduduki keadaan kuantum yang sama sesuai dengan asas pengecualian Pauli.[4]
Konsep muatan listrik yang tidak dapat dibagi-bagi lagi diteorikan untuk menjelaskan sifat-sifat kimiawi atom oleh filsuf alam Richard Laming pada awal tahun 1838;[6] nama electron diperkenalkan untuk menamakan muatan ini pada tahun 1894 oleh fisikawan Irlandia George Johnstone Stoney. Elektron berhasil diidentifikasikan sebagai partikel pada tahun 1897 oleh J. J. Thomson.[1][7]
Dalam banyak fenomena fisika, seperti listrik, magnetisme dan konduktivitas termal, elektron memainkan peran yang sangat penting. Suatu elektron yang bergerak relatif terhadap pengamat akan menghasilkan medan magnetik dan lintasan elektron tersebut juga akan dilengkungkan oleh medan magnetik eksternal. Ketika sebuah elektron dipercepat, ia dapat menyerap ataupun memancarkan energi dalam bentuk foton. Elektron bersama-sama dengan inti atom yang terdiri dari proton dan neutron, membentuk atom. Namun, elektron hanya mengambil 0,06% massa total atom. Gaya tarik Coulomb antara elektron dengan proton menyebabkan elektron terikat dalam atom. Pertukaran ataupun perkongsian elektron antara dua atau lebih atom merupakan sebab utama terjadinya ikatan kimia.[8]
Menurut teorinya, kebanyakan elektron dalam alam semesta diciptakan pada peristiwa Big Bang (ledakan besar), namun ia juga dapat diciptakan melalui peluruhan beta isotop radioaktif maupun dalam tumbukan berenergi tinggi, misalnya pada saat sinar kosmis memasuki atmosfer. Elektron dapat dihancurkan melalui pemusnahan dengan positron, maupun dapat diserap semasa nukleosintesis bintang. Peralatan-peralatan laboratorium modern dapat digunakan untuk memuat ataupun memantau elektron individual. Elektron memiliki banyak kegunaan dalam teknologi modern, misalnya dalam mikroskop elektron, terapi radiasi, dan pemercepat partikel.
Pada tahun 1737, C. F. du Fay dan Hawksbee secara independen menemukan apa yang mereka percaya sebagai dua jenis listrik friksional; satunya dihasilkan dari penggosokan gelas, yang lainnya dihasilkan dari penggosokan resin. Dari sinilah, Du Fay berteori bahwa listrik terdiri dari dua fluida elektris, yaitu "vitreous" dan "resinous", yang dipisahkan oleh gesekan dan menetralkan satu sama lainnya ketika bergabung.[11] Satu dasarwasa kemudian, Benjamin Franklin mengajukan bahwa listrik tidaklah berasal dari fluida elektris yang bermacam-macam, namun berasal dari fluida elektris yang sama di bawah tekanan yang berbeda. Ia memberikan tatanama muatan positif dan negatif untuk tekanan yang berbeda ini.[12][13]
Antara tahun 1838 dan 1851, filsuf alam Britania Richard Laming mengembangkan gagasan bahwa atom terdiri dari materi inti yang dikelilingi oleh partikel subatom yang memiliki muatan listrik.[14] Awal tahun 1846, fisikawan Jerman William Weber berteori bahwa listrik terdiri dari fluida yang bermuatan positif dan negatif, dan interaksinya mematuhi hukum kuadrat terbalik. Setelah mengkaji fenomena elektrolisis pada tahun 1874, fisikawan Irlandia George Johnstone Stoney mengajukan teori bahwa terdapat suatu "satuan kuantitas listrik tertentu" yang merupakan muatan sebuah ion monovalen. Ia berhasil memperkirakan nilai muatan elementer e ini menggunakan Hukum elektrolisis Faraday.[15] Namun, Stoney percaya bahwa muatan-muatan ini secara permanen terikat pada atom dan tidak dapat dilepaskan. Pada tahun 1881, fisikawan Jerman Hermann von Helmholtz berargumen bahwa baik muatan positif dan negatif dibagi menjadi beberapa bagian elementer, yang "berperilaku seperti atom dari listrik".[6]
Pada tahun 1894, Stoney menciptakan istilah electron untuk mewakili muatan elementer ini.[16] Kata electron merupakan kombinasi kata electric dengan akhiran on, yang digunakan sekarang untuk merujuk pada partikel subatomik seperti proton dan neutron.[17][18]
Fisikawan Britania kelahiran Jerman Arthur Schuster memperluas eksperimen Crookes dengan memasang dua pelat logam secara paralel terhadap sinar katode dan memberikan potensial listrik antara dua pelat tersebut. Medan ini kemudian membelokkan sinar menuju pelat bermuatan positif, memberikan bukti lebih jauh bahwa sinar ini mengandung muatan negatif. Dengan mengukur besar pembelokan sinar sesuai dengan arus listrik yang diberikan, pada tahun 1890, Schuster berhasil memperkirakan rasio massa terhadap muatan komponen-komponen sinar. Namun, perhitungan ini menghasilkan nilai yang seribu kali lebih besar daripada yang diperkirakan, sehingga perhitungan ini tidak dipercayai pada saat itu.[22][25]
Pada tahun 1896, fisikawan Britania J. J. Thomson, bersama dengan koleganya John S. Townsend dan H. A. Wilson,[1] melakukan eksperimen yang mengindikasikan bahwa sinar katode benar-benar merupakan partikel baru dan bukanlah gelombang, atom, ataupun molekul seperti yang dipercayai sebelumnya. Thomson membuat perkiraan yang cukup baik dalam menentukan muatan e dan massa m, dan menemukan bahwa partikel sinar katode, yang ia sebut "corpuscles" mungkin bermassa seperseribu massa ion terkecil yang pernah diketahui (hidrogen).[7] Ia menunjukkan bahwa nisbah massa terhadap muatan, e/m, tidak tergantung pada material katode. Ia lebih jauh lagi menunjukkan bahwa partikel bermuatan negatif yang dihasilkan oleh bahan-bahan radioaktif, bahan-bahan yang dipanaskan, atau bahan-bahan yang berpendar bersifat universal.[26] Nama elektron kemudian diajukan untuk menamakan partikel ini oleh fisikawan Irlandia George F. Fitzgerald, dan seterusnya mendapatkan penerimaan yang universal.[22]
Manakala sedang mengkaji mineral fluoresens pada tahun 1896, fisikawan Perancis Henri Becquerel menemukan bahwa mineral tersebut memancarkan radiasi tanpa terpapar sumber energi eksternal. Bahan radioaktif ini menarik perhatian banyak ilmuwan, meliputi ilmuwan Selandia Baru Ernest Rutherford yang menemukan bahwa partikel ini memancarkan partikel. Ia melabeli partikel ini partikel alfa dan partikel beta berdasarkan kemampuannya menembus materi.[27] Pada tahun 1900, Becquerel menunjukkan bahwa emisi sinar beta oleh radium dapat dibelokkan oleh medan listrik, dan rasio massa terhadap muatannya adalah sama dengan rasio massa terhadap muatan sinar katode.[28] Bukti ini menguatkan pandangan bahwa elektron merupakan komponen atom.[29][30]
Muatan elektron kemudian diukur lebih seksama lagi oleh fisikawan Amerika Robert Millikan dalam Percobaan tetesan minyak pada tahun 1909. Hasil percobaan ini dipublikasikan pada tahun 1911. Percobaan ini menggunakan medan listrik untuk mencegah tetesan minyak bermuatan jatuh sebagai akibat dari gravitasi. Peralatan yang digunakan dalam percobaan ini dapat mengukur muatan listrik dari 1–150 ion dengan batas kesalahan kurang dari 0,3%. Percobaan yang mirip dengan percobaan Millikan sebelumnya telah dilakukan oleh Thomson, menggunakan tetesan awan air bermuatan yang dihasilkan dari elektrolisis,[1] dan oleh Abram Ioffe pada tahun 1911, yang secara independen mendapatkan hasil yang sama dengan Millikan menggunakan mikropartikel logam bermuatan. Ia mempublikasikan hasil percobaannya pada tahun 1913.[31] Namun, tetesan minyak lebih stabil daripada tetesan air karena laju penguapan minyak yang lebih lambat, sehingga lebih cocok digunakan untuk percobaan dalam periode waktu yang lama.[32]
Sekitar permulaan abad ke-20, ditemukan bahwa di bawah kondisi tertentu, partikel bermuatan yang bergerak cepat dapat menyebabkan kondensasi uap air yang lewat jenuh di sepanjang lintasan partikel tersebut. pada tahun 1911, Charles Wilson menggunakan prinsip ini untuk membangun bilik kabut, mengijikan pelacakan partikel-partikel bermuatan seperti elektron yang bergerak cepat untuk difoto.[33]
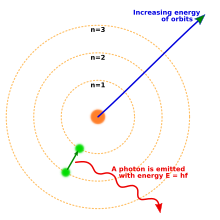
Pada tahun 1914, percobaan yang dilakukan oleh fisikawan Ernest Rutherford, Henry Moseley, James Franck dan Gustav Hertz secara garis besar telah berhasil membangun model struktur atom sebagai inti atom bermuatan positif yang dikelilingi oleh elektron bermassa kecil.[34] Pada tahun 1913, fisikawan Denmark Niels Bohr berpostulat bahwa elektron berada dalam keadaan energi terkuantisasi, dengan energinya ditentukan berdasarkan momentum sudut orbit elektron di sekitar inti. Elektron dapat berpindah dari satu keadaan ke keadaan lain (atau orbit) dengan memancarkan emisi ataupun menyerap foton pada frekuensi tertentu. Menggunakan model orbit terkuantisasi ini, ia secara akurat berhasil menjelaskan garis spektrum atom hidrogen.[35] Namun, model Bohr gagal menjelaskan intensitas relatif garis spektrum ini dan gagal pula dalam menjelaskan spektrum atom yang lebih kompleks.[34]
Ikatan kimia antaratom dijelaskan oleh Gilbert Newton Lewis, yang pada tahun 1916 mengajukan bahwa ikatan kovalen antara dua atom dijaga oleh sepasang elektron yang dibagikan di antara dua atom yang berikatan.[36] Kemudian, pada tahun 1923, Walter Heitler dan Fritz London memberikan penjelasan penuh mengenai formasi pasangan elektron dan ikatan kimia berdasarkan mekanika kuantum.[37] Pada tahun 1919, kimiawan Amerika Irving Langmuir menjabarkan lebih lanjut lagi model statis atom Lewis dan mengajukan bahwa semua elektron terdistribusikan dalam "kulit-kulit bola konsentris, kesemuannya berketebalan sama".[38] Kulit tersebut kemudian dibagi olehnya ke dalam sejumlah sel yang tiap-tiap sel mengandung sepasangan elektron. Dengan model ini, Langmuir berhasil secara kualitatif menjelaskan sifat-sifat kimia semua unsur dalam tabel periodik.[37]
Pada tahun 1924, fisikawan Austria Wolfang Pauli memperhatikan bahwa struktur seperi kulit atom ini dapat dijelaskan menggunakan empat parameter yang menentukan tiap-tiap keadaan energi kuantum sepanjang tiap keadaan diduduki oleh tidak lebih dari satu elektron tunggal. Pelarangan adanya lebih dari satu elektron menduduki keadaan energi kuantum yang sama dikenal sebagai asas pengecualian Pauli.)[39] Mekanisme fisika yang menjelaskan parameter keempat, yang memiliki dua nilai berbeda, diberikan oleh fisikawan Belanda Abraham Goudsmith dan George Uhlenbeck ketika mereka mengajukan bahwa elektron, selain momentum sudut orbitnya, juga dapat memiliki momentum sudut intrinsiknya sendiri.[34][40] Ciri ini kemudian dikenal sebagai spin, yang menjelaskan pemisahan garis spektrum yang terpantau pada spektrometer beresolusi tinggi. Fenomena ini dikenal sebagai pemisahan struktur halus.[41]

Dalam disertasi tahun 1924 berjudul Recherches sur la théorie des quanta (Riset mengenai Teori Kuantum), fisikawan Perancis Louis de Broglie berhipotesis bahwa semua materi memiliki gelombang De Broglie yang mirip dengan cahaya.[42] Ini berarti bahwa di bawah kondisi yang tepat, elektron dan semua materi dapat menunjukkan sifat-sifat seperti partikel maupun seperti gelombang. Sifat korpuskular partikel dapat didemonstrasikan ketika ia dapat ditunjukkan memiliki posisi terlokalisasi dalam ruang sepanjang trayektorinya pada waktu apapun.[43] Sifat seperti gelombang dapat dipantau ketika seberkas cahaya dilewatkan melalui celah-celah paralel dan menghasilkan pola-pola interferensi.
Pada tahun 1927, efek interferensi ini berhasil ditunjukkan juga berlaku bagi berkas elektron oleh fisikawan Inggris George Paget Thomson menggunakan film logam tipis dan oleh fisikawan Amerika Clinton Davisson dan Lester Germer menggunakan kristal nikel.[44] Suksesnya prediksi de Broglie turut membantu Erwin Schrödinger yang pada tahun 1926 mempublikasikan persamaan Schrödinger yang secara sukses mendeskripsikan bagaimana gelombang elektron merambat.[45] Daripada menghasilkan penyelesaian yang menentukan lokasi elektron seiring dengan berjalannya waktu, persamaan gelombang ini dapat digunakan untuk memprediksikan probabilitas penemuan sebuah elektron dekat sebuah posisi. Pendekatan ini kemudian disebut sebagai mekanika kuantum, yang memberikan perhitungan keadaan energi elektron atom hidrogen dengan sangat tepat. Ketika spin dan interaksi antara banyak elektron diperhitungkan, mekanika kuantum memungkinkan konfigurasi elektron dalam atom bernomor atom lebih tinggi daripada hidrogen diprediksi dengan tepat.[46]
Pada tahun 1928, berdasarkan karya Wolfgang Pauli, Paul Dirac menghasilkan model elektron, persamaan Dirac, yang konsisten dengan teori relativitas, dengan menerapkan pertimbangan relativitas dan simetri ke dalam perumusan Hamiltonan mekanika kuantum medan elektro-magnetik.[47] Agar dapat memecahkan berbagai masalah dalam persamaan relativistiknya, pada tahun 1930, Dirac mengembangkan model vakum sebagai lautan partikel tak terhingga yang berenergi negatif (dikenal sebagai laut Dirac). Ini mengantar Dirac memprediksikan keberadaan positron, antimateri dari elektron.[48] Partikel positron ditemukan pada tahun 1932 oleh Carl D. Anderson, yang menyerukan dinamakannya elektron biasa sebagai negatron, dan elektron digunakan sebagai istilah generik untuk merujuk pada kedua partikel tersebut. Penggunaan istilah 'negatron' kadang-kadang masih dapat ditemukan sekarang, dan dapat disingkat menjadi 'negaton'.[49][50]
Pada tahun 1947, Willis Lamb, berkolaborasi dengan murid pascasarjananya Robert Retherford, menemukan bahwa keadaan kuantum tertentu atom hidrogen, yang seharusnya berenergi sama, bergeser relatif terhadap satu sama lain. Pergesaran ini disebut sebagai geseran Lamb. Pada waktu yang bersamaan, Polykarp Kusch, bekerja dengan Henry M. Foley, menemukan bahwa momen magnetik elektron sedikit lebih besar daripada yang diprediksikan oleh teori Dirac. Perbedaan kecil ini kemudian disebut sebagai anomali momen dipol magnetik elektron. Untuk memecahkan masalah ini, teori yang disebut elektrodinamika kuantum dikembangkan oleh Sin-Itiro Tomonaga, Julian Schwinger dan Richard P. Feynman pada akhir tahun 1940-an.[51]
Dengan energi berkas sebesar 1,5 GeV, penumbuk partikel berenergi tinggi ADONE memulai operasinya pada tahun 1968.[54] Alat ini mempercepat elektron dan positron dengan arah yang berlawanan, secara efektif menggandakan energi tumbukan dibandingkan apabila menumbukkan elektron dengan target yang diam.[55] Large Electron-Positron Collider (LEP) di CERN yang beroperasi dari tahun 1989 sampai dengan tahun 2000 berhasil mencapai energi tumbukan sebesar 209 GeV dan berhasil membuat pengukuran untuk Model Standar fisika partikel.[56][57]
Elektron memiliki muatan listrik sebesar -1,602 × 10-19 coulomb,[60] yang digunakan sebagai satuan standar untuk muatan partikel subatom. Di bawah ambang batas keakuratan eksperimen, muatan elektron adalah sama dengan muatan proton, namun memiliki tanda positif.[63] Oleh karena simbol e digunakan untuk merujuk pada muatan elementer, elektron umumnya disimbolkan sebagai e−, dengan tanda minus mengindikasikan muatan negatif. Positron disimbolkan sebagai e+ karena ia memiliki ciri-ciri yang sama dengan elektron namun bermuatan positif.[60][59]
Elektron memiliki momentum sudut intrinsik atau spin senilai 1⁄2.[60] Sifat ini biasanya dinyatakan dengan merujuk elektron sebagai partikel spin-1⁄2.[59] Untuk partikel seperti ini, besaran spinnya adalah √3⁄2 ħ[cat 3] manakala hasil pengukuran proyeksi spin pada sumbu apapun hanyalah dapat bernilai ±ħ⁄2. Selain spin, elektron juga memiliki momen magnetik intrinsik di sepanjang sumbu spinnya.[60] Momen magnetik elektron kira-kira sama dengan satu magneton Bohr,[64][cat 4] dengan konstanta fisika sebesar 9,274 009 15(23) × 10−24 joule per tesla.[60] Orientasi spin terhadap momentum elektron menentukan helisitas partikel tersebut.[65]
Elektron tidak memiliki substruktur yang diketahui.[2][66] Oleh karena itu, ia didefinisikan ataupun diasumsikan sebagai partikel titik ataupun muatan titik dan tidak beruang.[4] Pemantaupaun pada satu elektron tunggal dalam perangkap Penning menunjukkan batasan atas jari-jari partikel sebesar 10−22 meter.[67] Terdapat sebuah tetapan fisika yang disebut sebagai "jari-jari elektron klasik" yang bernilai 2,8179 ×10-15 m. Namun terminologi ini berasal dari perhitungan sederhana yang mengabaikan efek-efek mekanika kuantum. Dalam kenyataannya, jari-jari elektron klasik tidak memiliki hubungan apapun dengan struktur dasar elektron.[68][cat 5]
Terdapat partikel elementer yang secara spontan meluruh menjadi partikel yang lebih ringan. Contohnya adalah muon yang meluruh menjadi elektron, neutrino, dan antineutrino, dengan waktu paruh rata-rata 2,2 × 10-6 detik. Namun, elektron diperkirakan stabil secara teoritis: elektron merupakan partikel teringan yang bermuatan, sehingga peluruhannya akan melanggar kekalan muatan.[69] Ambang bawah eksperimen untuk rata-rata umur paruh elektron adalah 4,6 × 1026 tahun, dengan taraf keyakinan sebesar 90%.[70]
Dalam kasus antisimetri, penyelesaian fungsi gelombang untuk elektron yang berinteraksi menghasilkan probabilitas yang bernilai nol untuk tiap pasangan elektron menduduki lokasi ataupun keadaan yang sama. Hal ini dikenal dengan nama asas pengecualian Pauli. Asas ini menjelaskan banyak sifat elektron.
Interaksi dengan partikel maya juga menjelaskan penyimpangan momen magnetik intrinsik elektron sebesar 0,1% dari magneton Bohr.[64][78] Kesesuaian yang sangat tepat antara perbedaan yang diprediksikan ini dengan nilai percobaan dipandang sebagai pencapaian besar elektrodinamika kuantum.[79]
Dalam fisika klasik, momentum sudut dan momen magnetik suatu objek bergantung pada dimensi fisikanya. Oleh karena itu, konsep elektron tak berdimensi yang memiliki momentum sudut dan momen magnetik tampaknya tidak konsisten. Paradoks ini dapat dijelaskan menggunakan pembentukan foton maya dalam medan listrik yang dihasilkan oleh elektron. Foton-foton maya ini menyebabkan elektron bergeser secara getar-getir (dinamakan Zitterbewegung),[80] yang mengakibatkan gerak melingkar dengan presesi. Gerak ini menghasilkan momen magnetik dan spin elektron.[4][81] Dalam atom, penciptaan foton maya ini menjelaskan geseran Lamb yang terpantau pada garis spektrum.[74]
Dalam elektrodinamika kuantum, interaksi elektromagnetik antara partikel dimediasi oleh foton. Elektron terisolasi yang tidak dipercepat tidak dapat memancar ataupun menyerap foton; apabila ia menyerap atau memancarkan foton, ini berarti pelanggaran hukum kekekalan energi dan momentum. Walau demikian, foton maya dapat mentransfer momentum antar dua partikel bermuatan. Adalah pertukaran foton maya ini yang menghasilkan gaya Coulomb.[87] Emisi energi dapat terjadi ketika elektron yang bergerak dibelokkan oleh sebuah partikel bermuatan seperti proton. Percepatan elektron menghasilkan pancaran radiasi Bremsstrahlung.[88]
Kekuatan relatif interaksi elektromagnetik antara dua partikel bermuatan seperti elektron dengan proton diberikan oleh konstanta struktur halus. Nilai konstanta ini tidak memiliki dimensi dan merupakan nisbah dua energi: energi elektrostatik tarikan (ataupun tolakan) pada pemisahan satu panjang gelombang Compton dengan energi rihat muatan. Ia bernilai α ≈ 7,297353 × 10-3, ataupun kira-kira sama dengan 1⁄137.[60]
Ketika elektron dan positron bertumbukan, keduanya akan memusnahkan satu sama lainnya, menghasilkan dua atau lebih sinar foton gama. Jika elektron dan positronnya memiliki momentum yang dapat diabaikan, atom positronium dapat terbentuk sebelum pemusnahan, menghasilkan dua atau tiga foton sinar gama berenergi sebesar 1,022 MeV.[91][92] Di sisi lain, foton berenergi tinggi dapat berubah menjadi elektron dan positron kembali dalam suatu proses yang dinamakan produksi pasangan, namun hanya terjadi dengan keberadaan partikel bermuatan di dekatnya, seperti inti atom.[93][94]

Elektron dapat terikat pada inti atom melalui gaya tarik menarik Coulomb. Suatu sistem berelektron banyak yang terikat pada inti atom disebut sebagai atom. Jika jumlah elektron berbeda dari muatan listrik inti, atom tersebut dinamakan sebagai ion. Perilaku elektron terikat yang seperti gelombang dideskripsikan menggunakan fungsi matematika yang disebut orbital atom. Tiap-tiap orbital atom memiliki satu set bilangan kuantumnya sendiri, yaitu energi, momentum sudut, dan proyeksi momentum sudut. Menurut asas pengecualian Pauli, tiap orbital hanya dapat diduduki oleh dua elektron, yang harus berbeda dalam bilangan kuantum spinnya.
Elektron dapat berpindah dari satu orbtial ke orbital lainnya melalui emisi ataupun absorpsi foton yang energinya sesuai dengan perbedaan potensial antar orbital.[95] Metode perpindahan orbital lainnya meliputi pertumbukan dengan partikel elektron lain dan efek Auger.[96] Agar dapat melepaskan diri dari atom, energi elektron haruslah ditingkatkan melebihi energi pengikatannya. Ini terjadi pada efek fotolistrik, di mana foton yang berenergi lebih tinggi dari energi ionisasi atom diserap oleh elektron.[97]
Momentum sudut orbital elektron terkuantisasi. Oleh karena elektron bermuatan, ia menghasilkan momen magnetik orbital yang proposional terhadap momentum sudut. Keseluruhan momen magnetik sebuah atom adalah setera dengan jumlah vektor momen magnetik orbital dan momen magnetik spin keseluruhan elektron dan inti atom. Namun, momen magnetik inti sangatlah kecil dan dapat diabaikan jika dibandingkan dengan elektron. Momen magnetik dari dua elektron yang menduduki orbital yang sama (disebut elektron berpasangan) akan saling meniadakan.[98]
Ikatan kimia antaratom terjadi sebagai akibat dari interaksi elektromagnetik, sebagaimana yang dijelaskan oleh hukum mekanika kuantum.[99] Ikatan yang terkuat terbentuk melalui perkongsian elektron maupun transfer elektron di antara atom-atom, mengizinkan terbentuknya molekul.[8] Dalam molekul, pegerakan elektron dipengaruhi oleh beberapa inti atom dan elektron menduduki orbital molekul, sama halnya dengan elektron yang menduduki orbital atom pada atom bebas.[100] Faktor mendasar pada struktur molekul adalah keberadaan pasangan elektron. Kedua elektron yang berpasangan memiliki spin yang berlawanan, mengizinkan keduanya menduduki orbital molekul yang sama tanpa melanggar asas pengecualian Pauli. Orbital-orbital molekul yang berbeda memiliki distribusi spasial rapatan elektron yang berbeda pula. Sebagai contohnya, pada elektron berpasangan yang terlibat dalam ikatan, elektron dapat ditemukan dengan probabilitas yang tinggi disekitar daerah inti atom tertentu yang sempit, manakala pada elektron berpasangan yang tidak terlibat dalam ikatan, ia dapat terdistribusi pada ruang yang luas di sekitar inti atom.[101]
Elektron tunggal yang bergerak dalam vakum diistilahkan sebagai elektron bebas. Elektron-elektron dalam logam juga berperilaku seolah-olah bebas. Dalam kenyataannya, partikel yang umumnya diistilahkan elektron dalam logam dan padatan lainnya merupakan kuasi-elektron-kuasi-partikel, yang memiliki muatan listrik, spin, dan momen magnetik yang sama dengan elektron asli, namun bermassa berbeda.[106] Ketika elektron bebas bergerak dalam vakum ataupun dalam logam, ia akan menghasilkan aliran muatan yang disebut sebagai arus listrik. Arus listrik ini kemudian akan menghasilkan medan magnetik. Sebaliknya, arus dapat diciptakan pula dengan mengubah medan magnetik. Interaksi ini dinyatakan secara matematis menggunakan persamaan Maxwell.[107]
Pada suhu tertentu, tiap-tiap material memiliki konduktivitas listrik yang menentukan nilai arus listriknya ketika potensial listrik dialirkan kepadanya. Contoh benda yang memiliki konduktivitas listrik yang baik (disebut konduktor) misalnya emas dan tembaga, sedangkan gelas dan teflon adalah konduktor yang buruk. Dalam material dielektrik, elektron tetap terikat pada atom penyusunnya dan material tersebut berperilaku seperti insulator. Sebaiknya logam memiliki struktur pita elektronik yang mengandung pita elektronik yang terisi sebagian. Keberadaan pita tersebut mengizinkan elektron dalam logam berperilaku seolah-olah bebas (elektron terdelokalisasi). Elektron yang terdelokalisasi ini tidak terikat pada atom apapun, sehingga ketika dialiri medan listrik, elektron tersebut akan bergerak bebas seperti gas (gas fermi)[108] melalui material tersebut seperti elektron bebas.
Oleh karena tumbukan antara elektron dengan atom, kecepatan hanyatan elektron dalam konduktor memiliki kisaran milimeter per detik. Namun, kecepatan rambatan elektron biasanya adalah sekitar 75% kecepatan cahaya.[109] This occurs because electrical signals propagate as a wave, with the velocity dependent on the dielectric constant of the material.[110]
Logam merupakan konduktor panas yang baik, utamanya disebabkan oleh elektron terdelokalisasi yang bebas untuk mentranspor energi termal antaratom. Namun, berbeda dengan konduktivitas listrik, konduktivitas termal logam hampir tidak tergantung pada suhu. Konduktivitas termal diekspresikan secara matematis menurut hukum Wiedemann-Franz,[108] yang menyatakan bahwa rasio konduktivitas termal terhadap konduktivitas listrik berbanding lurus terhadap temperatur. Kebalauan termal dalam kisi logam meningkatkan resistivitas listrik material, sehingganya membuat arus listrik tergantung pada temperatur.[111]
Ketika didinginkan di bawah temperatur kritis, material dapat mengalami transisi fase yang menyebabkannya kehilangan semua resistivitas arus listrik. Hal ini dinamakan superkonduktivitas. Dalam teori BCS, perilaku ini dimodelkan oleh pasangan elektron yang memasuki keadaan kuantum kondensat Bose-Einstein. Pasangan Cooper ini memiliki gerakan yang dikopling oleh materi sekitar via getaran kekisi yang disebut fonon, sehingga elektron dapat menghindari tumbukan dengan atom-atom material yang menciptakan hambatan listrik.[112] (Pasangan Cooper memiliki jari-jari sekitar 100 nm, sehingga dapat bertumpang tindih satu sama lain.)[113] Walaupun begitu, mekanisme mengenai bagaimana superkonduktor temperatur tinggi bekerja masih belumlah terpecahkan.
Elektron yang berada dalam padatan konduktor, yang sendirinya juga merupakan kuasipartikel, ketika dikungkung secara ketat pada temperatur yang mendekati nol absolut, akan berperilaku seolah-olah terbelah lebih jauh menjadi dua kuasipartikel: spinon dan holon.[114][115] Spinon memiliki spin dan momen magnetik, sedangkan holon memiliki muatan listrik.
 dengan v adalah kecepatan partikel. Energi kinetik Ke sebuah elektron yang bergerak dengan kecepatan v adalah:
dengan v adalah kecepatan partikel. Energi kinetik Ke sebuah elektron yang bergerak dengan kecepatan v adalah:
Oleh karena elektron dapat berperilaku seperti gelombang, ia akan memiliki karakteristik panjang gelombang de Broglie. Nilai ini adalah λe = h/p dengan h adalah konstanta Planck dan p adalah momentum.[42] Untuk 51 GeV elektron di atas, panjang gelombangnya adalah sekitar 2,4 × 10-17 m. Nilai ini cukup kecil untuk menjelajahi struktur yang lebih kecil dari inti atom.[118]
Semasa proses leptogenesis, terdapat jumlah elektron yang lebih banyak daripada positron. Sampai sekarang, masihlah belum jelas mengapa elektron dapat berjumlah lebih banyak daripada positron.[121] Sekitar satu dari satu milyar elektron lolos dari proses pemusnahan. Kelebihan jumlah proton dibandingkan antiproton juga terjadi dalam kondisi asimetri barion, menyebabkan muatan total alam semesta menjadi nol.[122][123] Proton dan neutron yang tidak musnah kemudian mulai berpartisipasi dalam reaksi nukleosintesis, membentuk isotop hidrogen dan helium, serta sekelumit litium. Proses ini mencapai puncaknya setelah lima menit.[124] Neutron yang tersisa kemudian menjalani peluruhan beta negatif dengan umur paruh sekitar seribu detik, melepaskan proton dan elektron dalam prosesnya,
Kira-kira satu juta tahun setelah big bang, generasi bintang pertama mulai terbentuk.[126] Dalam bintang, nukleosintesis bintang mengakibatkan pembentukan positron dari penggabungan inti atom. Partikel antimateri ini dengan segera memusnahkan elektron dan melepaskan sinar gama. Oleh sebab itu, terjadi penurunan jumlah elektron yang diikuti dengan peningkatan jumlah neutron dengan kuantitas yang sama. Walau demikian, proses evolusi bintang dapat pula mengakibatkan sintesis isotop-isotop radioaktif. Beberapa isotop tersebut kemudian dapat menjalani peluruhan beta negatif dan memancarkan elektron dan antineutrino dari inti atom.[127] Salah satu contohnya adalah isotop kobalt-60 (60Co) yang meluruh menjadi nikel-60 (60Ni).[128]
Pada akhir masa kehidupannya, bintang yang bermassa lebih dari 20 massa surya dapat menjalani keruntuhan gravitasi dan membentuk lubang hitam.[129] Menurut fisika klasik, objek luar angkasa yang sangat berat ini menghasilkan gaya tarik gravitasi yang sangat besar sehingganya tiada benda apapun, termasuk radiasi elektromagnetik, yang dapat lolos dari jari-jari Schwarzschild. Namun, dipercayai bahwa efek mekanika kuantum mengizinkan radiasi Hawking dipancarkan pada jarak ini. Elektron (dan positron) diperkirakan diciptakan di horizon persitiwa lubang hitam.
Ketika pasangan-pasangan partikel maya (seperti elektron dan positron) tercipta disekitar horizon peristiwa, distribusi spasial acak partikel-partikel ini mengizinkan salah satu partikel muncul pada bagian eksterior; proses ini disebut sebagai penerowongan kuantum. Potensial gravitasi lubang hitam kemudian dapat memasok energi yang mengubah partikel maya menjadi partikel nyata, mengizinkannya beradiasi keluar menuju luar angkasa.[130] Sebagai gantinya, pasangan lainnya akan mendapatkan energi negatif, yang menyebabkan penurunan massa-energi lubang hitam. Laju radiasi Hawking meningkat seiring dengan menurunnya massa, pada akhirnya akan menyebabkan lubang hitam "menguap" sampai akhirnya meledak.[131]
Sinar kosmis adalah partikel-partikel yang bergerak di luar angkasa dengan energi yang tinggi. Energi sebesar 3,0 × 1020 eV telah tercatat.[132] Ketika partikel-partikel ini bertumbukan dengan nukleon di atmosfer Bumi, hujanan partikel-partikel dihasilkan, termasuk pula pion.[133] Lebih dari setengah radiasi kosmis yang terpantau dari permukaan Bumi terdiri dari muon. Partikel ini merupakan sejenis lepton yang dihasilkan di atmosfer bagian atas melalui peluruhan pion. Muon, pada gilirannya, dapat meluruh menjadi elektron maupun positron. Oleh karena itu, untuk pion bermuatan negatif π−,[134]
Frekuensi sebuah foton berbanding lurus dengan energinya. Elektron yang terikat pada inti atom dengan aras energi tertentu akan menyerap ataupun memancarkan foton pada frekuensi aras energi tersebut. Contohnya, ketika atom diiradiasi oleh sumber energi berspektrum lebar, garis-garis absorpsi tertentu akan muncul pada spektrum radiasi yang ditransmisikan. Tiap-tiap unsur ataupun molekul yang berbeda akan menampakkan garis-garis spektrum yang berbeda-beda pula. Pengukuran spektroskopi terhadap kekuatan dan lebar garis-garis spektrum ini memungkinkan penentuan komposisi kimia dan sifat fisika suatu zat.[137][138]
Dalam laboratorium, interaksi elektron individu dapat dipantau menggunakan detektor partikel, yang memungkinkan pengukuran sifat-sifat fisika elektron seperti energi, spin, dan muatannya.[97] Dikembangkannya perangkap Paul dan perangkap Penning mengizinkan partikel bermuatan diperangkap ke dalam suatu daerah tertentu untuk masa yang lama. Hal ini mengizinkan pengukuran yang cermat mengenai sifat dan ciri partikel. Dalam satu percobaan, perangkap Penning dapat memerangkap satu elektron tunggal dalam periode waktu 10 bulan.[139] Momen magnetik elektron yang telah diukur, telah mencapai presisi pengukuran hingga 11 digit. Pada saat itu (1980), pengukuran ini lebih akurat daripada pengukuran konstanta fisika lainnya.[140]
Gambar video pertama yang memperlihatkan distribusi energi elektron direkam oleh sekelompok ilmuwan di Universitas Lund Swedia pada Februari 2008. Para ilmuwan ini menggunakan kilatan cahaya yang sangat pendek, disebut sebagai pulsa attosekon (10-18), mengizinkan gerak elektron dipantau untuk pertama kalinya.[141][142]
Distribusi elektron dalam material padat dapat divisualisasikan menggunakan ARPES (angle resolved photoemission spectroscopy). Teknik ini menggunakan efek fotolistrik untuk mengukur ruang timbal-balik, yaitu suatu representasi struktur periodik yang digunakan untuk menduga struktur awal material. ARPES dapat digunakan untuk menentukan arah, kecepatan, dan sebaran elektron dalam material.[143]

Berkas elektron digunakan dalam proses pengelasan,[145] yang mengizinkan rapatan energi sampai sebesar 107 W·cm−2 diterapkan pada sasaran sempit berdiameter 0,1–1,3 mm dan biasanya tidak memerlukan bahan isi. Teknik pengelasan ini harus dilakukan dalam kondisi vakum, sehingga berkas elektron tidak berinteraksi dengan gas sebelum mencapai target. Tekni ini dapat digunakan untuk menyatukan bahan-bahan konduktif yang tidak cocok dilas menggunakan teknik pengelasan biasa.[146][147]
Litografi berkas elektron (EBL) merupakan suatu metode pengetsaan semikonduktor dengan resolusi lebih kecil dari satu mikron.[148] Teknik ini berbiaya tinggi, lambat, dan perlu dioperasikan secara vakum dan cenderung mengakibatkan sebaran elektron pada padatan. Oleh karena sebaran ini, resolusinya terbatas pada 10 nm. Oleh karenanya, EBL utamanya digunakan pada produksi sejumlah kecil sirkuit terpadu yang terspesialisasi.[149]
Pemrosesan berkas elektron digunakan untuk mengiradiasi material agar sifat-sifat fisikanya berubah ataupun untuk tujuan sterilisasi produk makanan dan medis.[150] Dalam terapi radiasi berkas elektron dihasilkan oleh pemercepat liner untuk pengobatan tumor superfisial. Oleh karena berkas elektron hanya menembus kedalaman yang terbatas sebelum diserap, biasanya sampai dengan 5 cm untuk elektron berenergi 5–20 MeV, terapi elektron berguna untuk mengobati lesi kulit seperti karsinoma sel basal. Berkas elektron dapat digunakan untuk mensuplemen perawatan daerah-daerah yang telah diiradiasi oleh sinar-X.[151][152]
Pemercepat partikel menggunakan medan listrik untuk membelokkan elektron dan antipartikelnya mencapai energi tinggi. Oleh karena partikel ini bergerak melalui medan magnetik, ia memancarkan radiasi sinkrotron. Intensitas radiasi ini bergantung pada spin, yang menyebabkan polarisasi berkas elektron (dikenal sebagai efek Sokolov-Ternov). Berkas elektron yang terpolarisasi ini dapat digunakan dalam berbagai eksperimen. Radiasi sinkotron juga dapat digunakan untuk pendinginan berkas elektron, yang menurunkan sebaran momentum partikel. Seketika partikel telah dipercepat sampai pada energi yang ditentukan, elektron dan positron ditumbukkan. Emisi energi yang dihasilkan oleh tumbukan tersebut dipantau menggunakan detektor partikel dan dipelajari dalam fisika partikel.[153]
Mikroskop elektron mengarahkan berkas elektron yang difokuskan kepada suatu spesimen. Pada saat berkas berinteraksi dengan spesimen, beberapa elektron berubah sifatnya, misalnya pada arah pergerakan, sudut, energi, dan fase relatif elektron. Dengan mencatat perubahan pada berkas elektron, para ilmuwan dapat menghasilkan citra material yang diperbesar tersebut.[157]
Elektron, yang termasuk ke dalam generasi keluarga partikel lepton pertama,[4] berpartisipasi dalam interaksi gravitasi, interaksi elektromagnetik dan interaksi lemah.[5] Sama seperti semua materi, elektron memiliki sifat bak partikel maupun bak gelombang (dualitas gelombang-partikel), sehingga ia dapat bertumbukan dengan partikel lain dan berdifraksi seperti cahaya. Oleh karena elektron termasuk fermion, dua elektron berbeda tidak dapat menduduki keadaan kuantum yang sama sesuai dengan asas pengecualian Pauli.[4]
Konsep muatan listrik yang tidak dapat dibagi-bagi lagi diteorikan untuk menjelaskan sifat-sifat kimiawi atom oleh filsuf alam Richard Laming pada awal tahun 1838;[6] nama electron diperkenalkan untuk menamakan muatan ini pada tahun 1894 oleh fisikawan Irlandia George Johnstone Stoney. Elektron berhasil diidentifikasikan sebagai partikel pada tahun 1897 oleh J. J. Thomson.[1][7]
Dalam banyak fenomena fisika, seperti listrik, magnetisme dan konduktivitas termal, elektron memainkan peran yang sangat penting. Suatu elektron yang bergerak relatif terhadap pengamat akan menghasilkan medan magnetik dan lintasan elektron tersebut juga akan dilengkungkan oleh medan magnetik eksternal. Ketika sebuah elektron dipercepat, ia dapat menyerap ataupun memancarkan energi dalam bentuk foton. Elektron bersama-sama dengan inti atom yang terdiri dari proton dan neutron, membentuk atom. Namun, elektron hanya mengambil 0,06% massa total atom. Gaya tarik Coulomb antara elektron dengan proton menyebabkan elektron terikat dalam atom. Pertukaran ataupun perkongsian elektron antara dua atau lebih atom merupakan sebab utama terjadinya ikatan kimia.[8]
Menurut teorinya, kebanyakan elektron dalam alam semesta diciptakan pada peristiwa Big Bang (ledakan besar), namun ia juga dapat diciptakan melalui peluruhan beta isotop radioaktif maupun dalam tumbukan berenergi tinggi, misalnya pada saat sinar kosmis memasuki atmosfer. Elektron dapat dihancurkan melalui pemusnahan dengan positron, maupun dapat diserap semasa nukleosintesis bintang. Peralatan-peralatan laboratorium modern dapat digunakan untuk memuat ataupun memantau elektron individual. Elektron memiliki banyak kegunaan dalam teknologi modern, misalnya dalam mikroskop elektron, terapi radiasi, dan pemercepat partikel.
Sejarah
Orang Yunani Kuno memperhatikan bahwa ambar dapat menarik benda-benda kecil ketika digosok-gosokkan dengan bulu hewan. Selain petir, fenomena ini merupakan salah satu catatan terawal manusia mengenai listrik.[9] Dalam karya tahun 1600-nya De Magnete, fisikawan Inggris William Gilbert menciptakan istilah baru electricus untuk merujuk pada sifat penarikan benda-benda kecil setelah digosok.[10] Bahasa Inggris untuk kata electric diturunkan dari bahasa Latin ēlectrum, yang berasal dari bahasa Yunani ήλεκτρον (ēlektron) untuk batu ambar.Pada tahun 1737, C. F. du Fay dan Hawksbee secara independen menemukan apa yang mereka percaya sebagai dua jenis listrik friksional; satunya dihasilkan dari penggosokan gelas, yang lainnya dihasilkan dari penggosokan resin. Dari sinilah, Du Fay berteori bahwa listrik terdiri dari dua fluida elektris, yaitu "vitreous" dan "resinous", yang dipisahkan oleh gesekan dan menetralkan satu sama lainnya ketika bergabung.[11] Satu dasarwasa kemudian, Benjamin Franklin mengajukan bahwa listrik tidaklah berasal dari fluida elektris yang bermacam-macam, namun berasal dari fluida elektris yang sama di bawah tekanan yang berbeda. Ia memberikan tatanama muatan positif dan negatif untuk tekanan yang berbeda ini.[12][13]
Antara tahun 1838 dan 1851, filsuf alam Britania Richard Laming mengembangkan gagasan bahwa atom terdiri dari materi inti yang dikelilingi oleh partikel subatom yang memiliki muatan listrik.[14] Awal tahun 1846, fisikawan Jerman William Weber berteori bahwa listrik terdiri dari fluida yang bermuatan positif dan negatif, dan interaksinya mematuhi hukum kuadrat terbalik. Setelah mengkaji fenomena elektrolisis pada tahun 1874, fisikawan Irlandia George Johnstone Stoney mengajukan teori bahwa terdapat suatu "satuan kuantitas listrik tertentu" yang merupakan muatan sebuah ion monovalen. Ia berhasil memperkirakan nilai muatan elementer e ini menggunakan Hukum elektrolisis Faraday.[15] Namun, Stoney percaya bahwa muatan-muatan ini secara permanen terikat pada atom dan tidak dapat dilepaskan. Pada tahun 1881, fisikawan Jerman Hermann von Helmholtz berargumen bahwa baik muatan positif dan negatif dibagi menjadi beberapa bagian elementer, yang "berperilaku seperti atom dari listrik".[6]
Pada tahun 1894, Stoney menciptakan istilah electron untuk mewakili muatan elementer ini.[16] Kata electron merupakan kombinasi kata electric dengan akhiran on, yang digunakan sekarang untuk merujuk pada partikel subatomik seperti proton dan neutron.[17][18]
[sunting] Penemuan elektron
Fisikawan Jerman Johann Wilhelm Hittorf melakukan kajian mengenai konduktivitas listrik dalam gas. Pada tahun 1869, ia menemukan sebuah pancaran yang dipancarkan dari katode yang ukurannya meningkat seiring dengan menurunnya tekanan gas. Pada tahun 1876, fisikawan Jerman Eugen Goldstein menunjukkan bahwa sinar pancaran ini menghasilkan bayangnya, dan ia menamakannya sinar katode.[20] Semasa tahun 1870-an, kimiawan dan fisikawan Inggris William Crookes mengembangkan tabung katode pertama yang vakum.[21] Ia kemudian menunjukkan sinar berpendar yang tampak di dalam tabung tersebut membawa energi dan bergerak dari katode ke anode. Lebih jauh lagi, menggunakan medan magnetik, ia dapat membelokkan sinar tersebut dan mendemonstrasikan bahwa berkas ini berperilaku seolah-olah ia bermuatan negatif.[22][23] Pada athun 1879, ia mengajukan bahwa sifat-sifat ini dapat dijelaskan menggunakan apa yang ia istilahkan sebagai 'materi radian' (radiant matter). Ia mengajukan ini adalah keadaan materi keempat, yang terdiri dari molekul-molekul bermuatan negatif yang diproyeksikan dengan kecepatan tinggi dari katode.[24]
Fisikawan Britania kelahiran Jerman Arthur Schuster memperluas eksperimen Crookes dengan memasang dua pelat logam secara paralel terhadap sinar katode dan memberikan potensial listrik antara dua pelat tersebut. Medan ini kemudian membelokkan sinar menuju pelat bermuatan positif, memberikan bukti lebih jauh bahwa sinar ini mengandung muatan negatif. Dengan mengukur besar pembelokan sinar sesuai dengan arus listrik yang diberikan, pada tahun 1890, Schuster berhasil memperkirakan rasio massa terhadap muatan komponen-komponen sinar. Namun, perhitungan ini menghasilkan nilai yang seribu kali lebih besar daripada yang diperkirakan, sehingga perhitungan ini tidak dipercayai pada saat itu.[22][25]
Pada tahun 1896, fisikawan Britania J. J. Thomson, bersama dengan koleganya John S. Townsend dan H. A. Wilson,[1] melakukan eksperimen yang mengindikasikan bahwa sinar katode benar-benar merupakan partikel baru dan bukanlah gelombang, atom, ataupun molekul seperti yang dipercayai sebelumnya. Thomson membuat perkiraan yang cukup baik dalam menentukan muatan e dan massa m, dan menemukan bahwa partikel sinar katode, yang ia sebut "corpuscles" mungkin bermassa seperseribu massa ion terkecil yang pernah diketahui (hidrogen).[7] Ia menunjukkan bahwa nisbah massa terhadap muatan, e/m, tidak tergantung pada material katode. Ia lebih jauh lagi menunjukkan bahwa partikel bermuatan negatif yang dihasilkan oleh bahan-bahan radioaktif, bahan-bahan yang dipanaskan, atau bahan-bahan yang berpendar bersifat universal.[26] Nama elektron kemudian diajukan untuk menamakan partikel ini oleh fisikawan Irlandia George F. Fitzgerald, dan seterusnya mendapatkan penerimaan yang universal.[22]
Manakala sedang mengkaji mineral fluoresens pada tahun 1896, fisikawan Perancis Henri Becquerel menemukan bahwa mineral tersebut memancarkan radiasi tanpa terpapar sumber energi eksternal. Bahan radioaktif ini menarik perhatian banyak ilmuwan, meliputi ilmuwan Selandia Baru Ernest Rutherford yang menemukan bahwa partikel ini memancarkan partikel. Ia melabeli partikel ini partikel alfa dan partikel beta berdasarkan kemampuannya menembus materi.[27] Pada tahun 1900, Becquerel menunjukkan bahwa emisi sinar beta oleh radium dapat dibelokkan oleh medan listrik, dan rasio massa terhadap muatannya adalah sama dengan rasio massa terhadap muatan sinar katode.[28] Bukti ini menguatkan pandangan bahwa elektron merupakan komponen atom.[29][30]
Muatan elektron kemudian diukur lebih seksama lagi oleh fisikawan Amerika Robert Millikan dalam Percobaan tetesan minyak pada tahun 1909. Hasil percobaan ini dipublikasikan pada tahun 1911. Percobaan ini menggunakan medan listrik untuk mencegah tetesan minyak bermuatan jatuh sebagai akibat dari gravitasi. Peralatan yang digunakan dalam percobaan ini dapat mengukur muatan listrik dari 1–150 ion dengan batas kesalahan kurang dari 0,3%. Percobaan yang mirip dengan percobaan Millikan sebelumnya telah dilakukan oleh Thomson, menggunakan tetesan awan air bermuatan yang dihasilkan dari elektrolisis,[1] dan oleh Abram Ioffe pada tahun 1911, yang secara independen mendapatkan hasil yang sama dengan Millikan menggunakan mikropartikel logam bermuatan. Ia mempublikasikan hasil percobaannya pada tahun 1913.[31] Namun, tetesan minyak lebih stabil daripada tetesan air karena laju penguapan minyak yang lebih lambat, sehingga lebih cocok digunakan untuk percobaan dalam periode waktu yang lama.[32]
Sekitar permulaan abad ke-20, ditemukan bahwa di bawah kondisi tertentu, partikel bermuatan yang bergerak cepat dapat menyebabkan kondensasi uap air yang lewat jenuh di sepanjang lintasan partikel tersebut. pada tahun 1911, Charles Wilson menggunakan prinsip ini untuk membangun bilik kabut, mengijikan pelacakan partikel-partikel bermuatan seperti elektron yang bergerak cepat untuk difoto.[33]
[sunting] Teori atom

Model atom Bohr, menunjukkan keadaan elektron dengan energi terkuantisasi n. Sebuah elektron yang jatuh ke orbit bawah memancarkan foton yang energinya sama dengan selisih energi antar orbit.
Ikatan kimia antaratom dijelaskan oleh Gilbert Newton Lewis, yang pada tahun 1916 mengajukan bahwa ikatan kovalen antara dua atom dijaga oleh sepasang elektron yang dibagikan di antara dua atom yang berikatan.[36] Kemudian, pada tahun 1923, Walter Heitler dan Fritz London memberikan penjelasan penuh mengenai formasi pasangan elektron dan ikatan kimia berdasarkan mekanika kuantum.[37] Pada tahun 1919, kimiawan Amerika Irving Langmuir menjabarkan lebih lanjut lagi model statis atom Lewis dan mengajukan bahwa semua elektron terdistribusikan dalam "kulit-kulit bola konsentris, kesemuannya berketebalan sama".[38] Kulit tersebut kemudian dibagi olehnya ke dalam sejumlah sel yang tiap-tiap sel mengandung sepasangan elektron. Dengan model ini, Langmuir berhasil secara kualitatif menjelaskan sifat-sifat kimia semua unsur dalam tabel periodik.[37]
Pada tahun 1924, fisikawan Austria Wolfang Pauli memperhatikan bahwa struktur seperi kulit atom ini dapat dijelaskan menggunakan empat parameter yang menentukan tiap-tiap keadaan energi kuantum sepanjang tiap keadaan diduduki oleh tidak lebih dari satu elektron tunggal. Pelarangan adanya lebih dari satu elektron menduduki keadaan energi kuantum yang sama dikenal sebagai asas pengecualian Pauli.)[39] Mekanisme fisika yang menjelaskan parameter keempat, yang memiliki dua nilai berbeda, diberikan oleh fisikawan Belanda Abraham Goudsmith dan George Uhlenbeck ketika mereka mengajukan bahwa elektron, selain momentum sudut orbitnya, juga dapat memiliki momentum sudut intrinsiknya sendiri.[34][40] Ciri ini kemudian dikenal sebagai spin, yang menjelaskan pemisahan garis spektrum yang terpantau pada spektrometer beresolusi tinggi. Fenomena ini dikenal sebagai pemisahan struktur halus.[41]
[sunting] Mekanika kuantum

Dalam mekanika kuantum, perilaku elektron dalam atom dijelaskan menggunakan orbital, yang merupakan sebuah distribusi probabilitas dan bukannya orbit. Pada gambar di atas, bagian berwarna menunjukkan probabilitas relatif "penemuan" elektron yang memiliki energi sesuai dengan bilangan kuantum pada titik tersebut.
Pada tahun 1927, efek interferensi ini berhasil ditunjukkan juga berlaku bagi berkas elektron oleh fisikawan Inggris George Paget Thomson menggunakan film logam tipis dan oleh fisikawan Amerika Clinton Davisson dan Lester Germer menggunakan kristal nikel.[44] Suksesnya prediksi de Broglie turut membantu Erwin Schrödinger yang pada tahun 1926 mempublikasikan persamaan Schrödinger yang secara sukses mendeskripsikan bagaimana gelombang elektron merambat.[45] Daripada menghasilkan penyelesaian yang menentukan lokasi elektron seiring dengan berjalannya waktu, persamaan gelombang ini dapat digunakan untuk memprediksikan probabilitas penemuan sebuah elektron dekat sebuah posisi. Pendekatan ini kemudian disebut sebagai mekanika kuantum, yang memberikan perhitungan keadaan energi elektron atom hidrogen dengan sangat tepat. Ketika spin dan interaksi antara banyak elektron diperhitungkan, mekanika kuantum memungkinkan konfigurasi elektron dalam atom bernomor atom lebih tinggi daripada hidrogen diprediksi dengan tepat.[46]
Pada tahun 1928, berdasarkan karya Wolfgang Pauli, Paul Dirac menghasilkan model elektron, persamaan Dirac, yang konsisten dengan teori relativitas, dengan menerapkan pertimbangan relativitas dan simetri ke dalam perumusan Hamiltonan mekanika kuantum medan elektro-magnetik.[47] Agar dapat memecahkan berbagai masalah dalam persamaan relativistiknya, pada tahun 1930, Dirac mengembangkan model vakum sebagai lautan partikel tak terhingga yang berenergi negatif (dikenal sebagai laut Dirac). Ini mengantar Dirac memprediksikan keberadaan positron, antimateri dari elektron.[48] Partikel positron ditemukan pada tahun 1932 oleh Carl D. Anderson, yang menyerukan dinamakannya elektron biasa sebagai negatron, dan elektron digunakan sebagai istilah generik untuk merujuk pada kedua partikel tersebut. Penggunaan istilah 'negatron' kadang-kadang masih dapat ditemukan sekarang, dan dapat disingkat menjadi 'negaton'.[49][50]
Pada tahun 1947, Willis Lamb, berkolaborasi dengan murid pascasarjananya Robert Retherford, menemukan bahwa keadaan kuantum tertentu atom hidrogen, yang seharusnya berenergi sama, bergeser relatif terhadap satu sama lain. Pergesaran ini disebut sebagai geseran Lamb. Pada waktu yang bersamaan, Polykarp Kusch, bekerja dengan Henry M. Foley, menemukan bahwa momen magnetik elektron sedikit lebih besar daripada yang diprediksikan oleh teori Dirac. Perbedaan kecil ini kemudian disebut sebagai anomali momen dipol magnetik elektron. Untuk memecahkan masalah ini, teori yang disebut elektrodinamika kuantum dikembangkan oleh Sin-Itiro Tomonaga, Julian Schwinger dan Richard P. Feynman pada akhir tahun 1940-an.[51]
[sunting] Pemercepat partikel
Dengan berkembangnya pemercepat partikel semasa paruh pertama abad ke-20, fisikawan mulai mengkaji lebih dalam sifat-sifat partikel subatom.[52] Usaha pertama yang berhasil mempercepat elektron menggunakan induksi elektromagnetik dilakukan pada tahun 1942 oleh Donald Kerst. Betatron awalnya mencapai energi sebesar 2,3 MeV, manakala betatron-betatron selanjutnya berhasil mencapai 300 MeV. Pada tahun 1947, radiasi sinkrotron ditemukan menggunakan sinkrotron elektron 70 MeV di General Electric. Radiasi ini disebabkan oleh percepatan elektron yang bergerak mendekati kecepatan cahaya melalui medan magnetik.[53]Dengan energi berkas sebesar 1,5 GeV, penumbuk partikel berenergi tinggi ADONE memulai operasinya pada tahun 1968.[54] Alat ini mempercepat elektron dan positron dengan arah yang berlawanan, secara efektif menggandakan energi tumbukan dibandingkan apabila menumbukkan elektron dengan target yang diam.[55] Large Electron-Positron Collider (LEP) di CERN yang beroperasi dari tahun 1989 sampai dengan tahun 2000 berhasil mencapai energi tumbukan sebesar 209 GeV dan berhasil membuat pengukuran untuk Model Standar fisika partikel.[56][57]
[sunting] Karakteristik
[sunting] Klasifikasi
Dalam Model Standar fisika partikel, elektron termasuk ke dalam golongan partikel subatom yang disebut lepton, yang dipercayai sebagai partikel elementer. Elektron memiliki massa yang terendah di antara lepton bermuatan lainnya dan termasuk ke dalam partikel elementer generasi pertama.[58] Generasi kedua dan ketiganya mengandung lepton bermuatan, yaitu muon dan tauon, yang identik dengan elektron dalam hal muatannya, spin, dan interaksinya, terkecuali keduanya bermassa lebih besar. Lepton berbeda dari konstituen materi lainnya seperti kuark karena lepton tidak memiliki interaksi kuat. Semua anggota golongan lepton adalah termask fermion karena semuanya memiliki spin 1⁄2.[59][sunting] Ciri-ciri fundamental
Massa invarian sebuah elektron adalah kira-kira 9,109 × 10-31 kilogram,[60] ataupun setara dengan 5,489 × 10-4 satuan massa atom. Berdasarkan prinsip kesetaraan massa-energi Einstein, massa ini setara dengan energi rihat 0,511 MeV. Rasio antara massa proton dengan massa elektron adalah sekitar 1836.[3][61] Pengukuran astronomi menunjukkan bahwa rasio massa proton terhadap elektron tetap bernilai sama paling tidak selama setengah usia alam semesta, seperti yang diprediksikan oleh Model Standar.[62]Elektron memiliki muatan listrik sebesar -1,602 × 10-19 coulomb,[60] yang digunakan sebagai satuan standar untuk muatan partikel subatom. Di bawah ambang batas keakuratan eksperimen, muatan elektron adalah sama dengan muatan proton, namun memiliki tanda positif.[63] Oleh karena simbol e digunakan untuk merujuk pada muatan elementer, elektron umumnya disimbolkan sebagai e−, dengan tanda minus mengindikasikan muatan negatif. Positron disimbolkan sebagai e+ karena ia memiliki ciri-ciri yang sama dengan elektron namun bermuatan positif.[60][59]
Elektron memiliki momentum sudut intrinsik atau spin senilai 1⁄2.[60] Sifat ini biasanya dinyatakan dengan merujuk elektron sebagai partikel spin-1⁄2.[59] Untuk partikel seperti ini, besaran spinnya adalah √3⁄2 ħ[cat 3] manakala hasil pengukuran proyeksi spin pada sumbu apapun hanyalah dapat bernilai ±ħ⁄2. Selain spin, elektron juga memiliki momen magnetik intrinsik di sepanjang sumbu spinnya.[60] Momen magnetik elektron kira-kira sama dengan satu magneton Bohr,[64][cat 4] dengan konstanta fisika sebesar 9,274 009 15(23) × 10−24 joule per tesla.[60] Orientasi spin terhadap momentum elektron menentukan helisitas partikel tersebut.[65]
Elektron tidak memiliki substruktur yang diketahui.[2][66] Oleh karena itu, ia didefinisikan ataupun diasumsikan sebagai partikel titik ataupun muatan titik dan tidak beruang.[4] Pemantaupaun pada satu elektron tunggal dalam perangkap Penning menunjukkan batasan atas jari-jari partikel sebesar 10−22 meter.[67] Terdapat sebuah tetapan fisika yang disebut sebagai "jari-jari elektron klasik" yang bernilai 2,8179 ×10-15 m. Namun terminologi ini berasal dari perhitungan sederhana yang mengabaikan efek-efek mekanika kuantum. Dalam kenyataannya, jari-jari elektron klasik tidak memiliki hubungan apapun dengan struktur dasar elektron.[68][cat 5]
Terdapat partikel elementer yang secara spontan meluruh menjadi partikel yang lebih ringan. Contohnya adalah muon yang meluruh menjadi elektron, neutrino, dan antineutrino, dengan waktu paruh rata-rata 2,2 × 10-6 detik. Namun, elektron diperkirakan stabil secara teoritis: elektron merupakan partikel teringan yang bermuatan, sehingga peluruhannya akan melanggar kekalan muatan.[69] Ambang bawah eksperimen untuk rata-rata umur paruh elektron adalah 4,6 × 1026 tahun, dengan taraf keyakinan sebesar 90%.[70]
[sunting] Sifat-sifat kuantum
Seperti semua partikel, elektron dapat berperilaku seperti gelombang. Ini disebut sebagai dualitas gelombang-partikel dan dapat ditunjukkan menggunakan percobaan celah ganda. Sifat bak gelombang elektron mengizinkannya melewati kedua celah paralel secara bersamaan dan bukannya hanya melewati satu celah. Dalam mekanika kuantum, sifat bak gelombang suatu partikel dapat dideskripsikan secara matematis sebagai fungsi bernilai kompleks yang disebut sebagai fungsi gelombang (ψ). Ketika nilai mutlak fungsi ini di kuadratkan, nilai pengkuadratan ini akan memberikan probabilitas pemantauan suatu partikel dekat seuatu lokasi, disebut sebagai rapatan probabilitas.[71]Elektron yang satu dengan elektron yang lainnya tidak dapat dibedakan karena sifat fisika intrinsiknya. Dalam mekanika kuantum, hal ini berarti bahwa sepasang elektron yang berinteraksi haruslah dapat bertukar posisi tanpa adanya perubahan keadaan sistem yang terpantau. Fungsi gelombang fermion, termasuk pula elektron, adalah antisimetrik, berarti bahwa ia berubah tanda ketika dua elektron bertukaran; yakni ψ(r1, r2) = −ψ(r2, r1), dengan variabel r1 dan r2 adalah elektron pertama dan kedua. Oleh karena nilai mutlak tidak berubah ketika berubah tanda, ini berarti bahwa terdapat probabilitas yang tidak berubah. Berbeda dengan fermion, boson seperti foton memiliki fungsi gelombang simterik.[71]
Dalam kasus antisimetri, penyelesaian fungsi gelombang untuk elektron yang berinteraksi menghasilkan probabilitas yang bernilai nol untuk tiap pasangan elektron menduduki lokasi ataupun keadaan yang sama. Hal ini dikenal dengan nama asas pengecualian Pauli. Asas ini menjelaskan banyak sifat elektron.
[sunting] Partikel maya
Para fisikawan percaya bahwa ruang kosong mungkin secara berkesinambungan menciptakan banyak pasang partikel maya seperti positron dengan elektron, yang dengan cepat memusnahkan satu sama lainnya setelah tercipta.[72] Kombinasi variasi energi yang diperlukan untuk menciptakan partikel-partikel ini beserta waktu keberadaan partikel ini berada dalam ambang pendeteksian seperti yang dinyatakan oleh Prinsip ketidakpastian Heisenberg, ΔE·Δt ≥ ħ. Energi yang diperlukan untuk menciptakan partikel maya ini, ΔE, dapat "dipinjam" dari keadaan vakum untuk periode waktu Δt, sedemikian perkalian keduanya tidak lebih dari nilai konstanta Planck tereduksi, ħ ≈ 6,6 × 10-16 eV·s. Sehingga untuk elektron maya, Δt terlamanya adalah 1,3 × 10-21 s.[73]Ketika pasangan elektron-positron maya terbentuk, gaya coulomb dari medan listrik sekitar elektron menyebabkan positron yang tercipta tertarik ke elektron awal manakala elektron yang tercipta mengalami gaya tolak. Ini menyebabkan polarisasi vakum. Pada dasarnya, keadaan vakum berperilaku seperti media yang memiliki permitivitas dielektrik lebih besar dari satu. Sehingga muatan efektif sebuah elektron biasanya lebih kecil daripada nilai aslinya, dan muatan akan berkurang dengan meningkatnya jarak dari elektron.[74][75] Polarisasi ini dikonfirmasi secara eksperimental pada tahun 1997 menggunakan pemercepat partikel Jepang.[76] Partikel-partikel maya menyebabkan efek pemerisaian untuk massa elektron.[77]
Interaksi dengan partikel maya juga menjelaskan penyimpangan momen magnetik intrinsik elektron sebesar 0,1% dari magneton Bohr.[64][78] Kesesuaian yang sangat tepat antara perbedaan yang diprediksikan ini dengan nilai percobaan dipandang sebagai pencapaian besar elektrodinamika kuantum.[79]
Dalam fisika klasik, momentum sudut dan momen magnetik suatu objek bergantung pada dimensi fisikanya. Oleh karena itu, konsep elektron tak berdimensi yang memiliki momentum sudut dan momen magnetik tampaknya tidak konsisten. Paradoks ini dapat dijelaskan menggunakan pembentukan foton maya dalam medan listrik yang dihasilkan oleh elektron. Foton-foton maya ini menyebabkan elektron bergeser secara getar-getir (dinamakan Zitterbewegung),[80] yang mengakibatkan gerak melingkar dengan presesi. Gerak ini menghasilkan momen magnetik dan spin elektron.[4][81] Dalam atom, penciptaan foton maya ini menjelaskan geseran Lamb yang terpantau pada garis spektrum.[74]
[sunting] Interaksi
Elektron menghasilkan medan listrik yang menarik partikel bermuatan positif seperti proton dan menolak partikel lain yang bermuatan negatif. Kekuatan gaya tarik/tolak ini ditentukan oleh Hukum Coulomb.[82] Ketika elektron bergerak, ia menghasilkan medan magnetik.[83] Hukum Ampère-Maxwell menghubungkan medan magnetik dengan gerak massa elektron (arus listrik) terhadap seorang pengamat. Medan elektromagnetik partikel bermuatan yang bergerak diekspresikan menggunakan potensial Liénard–Wiechert, yang berlaku bahkan untuk partikel yang bergerak mendekati kecepatan cahaya.Ketika sebuah elektron bergerak melalui medan magnetik, gaya Lorentz akan memengaruhi arah lintasan elektron tegak lurus terhadap bidang medan magnet dan kecepatan elektron. Gaya sentripetal ini menyebabkan lintasan elektron berbentuk heliks. Percepatan yang dihasilkan dari gerak melengkung ini menginduksi elektron untuk memancarkan energi dalam bentuk radiasi sinkrotron.[84][85][cat 6] Emisi energi ini kemudian dapat mementalkan elektron, dikenal sebagai Gaya Abraham-Lorentz-Dirac, yang menciptakan gesekan yang memperlambat elektron. Gaya ini disebabkan oleh reaksi balik medan elektron terhadap dirinya sendiri.[86]
Dalam elektrodinamika kuantum, interaksi elektromagnetik antara partikel dimediasi oleh foton. Elektron terisolasi yang tidak dipercepat tidak dapat memancar ataupun menyerap foton; apabila ia menyerap atau memancarkan foton, ini berarti pelanggaran hukum kekekalan energi dan momentum. Walau demikian, foton maya dapat mentransfer momentum antar dua partikel bermuatan. Adalah pertukaran foton maya ini yang menghasilkan gaya Coulomb.[87] Emisi energi dapat terjadi ketika elektron yang bergerak dibelokkan oleh sebuah partikel bermuatan seperti proton. Percepatan elektron menghasilkan pancaran radiasi Bremsstrahlung.[88]
Tumbukan lenting antara sebuah foton (cahaya) dengan sebuah elektron bebas disebut sebagai hamburan Compton. Tumbukan ini menghasilkan transfer momentum dan transfer energi antar partikel, yang mengubah panjang gelombang foton sejumlah geseran Compton.[cat 7] Besaran maksimum geseran panjang gelombang ini adalah h/mec, yang dikenal sebagai panjang gelombang Compton.[89] Untuk sebuah elektron, ini bernilai 2,43 × 10−12 m.[60] Apabila panjang gelombang cahayanya panjang (contohnya panjang gelombang cahaya tampak adalah 0,4–0,7 μm), geseran panjang gelombang menjadi sangat kecil. Interaksi antara cahaya dengan elektron bebas seperti ini disebut sebagai hamburan Thomson.[90]
Kekuatan relatif interaksi elektromagnetik antara dua partikel bermuatan seperti elektron dengan proton diberikan oleh konstanta struktur halus. Nilai konstanta ini tidak memiliki dimensi dan merupakan nisbah dua energi: energi elektrostatik tarikan (ataupun tolakan) pada pemisahan satu panjang gelombang Compton dengan energi rihat muatan. Ia bernilai α ≈ 7,297353 × 10-3, ataupun kira-kira sama dengan 1⁄137.[60]
Ketika elektron dan positron bertumbukan, keduanya akan memusnahkan satu sama lainnya, menghasilkan dua atau lebih sinar foton gama. Jika elektron dan positronnya memiliki momentum yang dapat diabaikan, atom positronium dapat terbentuk sebelum pemusnahan, menghasilkan dua atau tiga foton sinar gama berenergi sebesar 1,022 MeV.[91][92] Di sisi lain, foton berenergi tinggi dapat berubah menjadi elektron dan positron kembali dalam suatu proses yang dinamakan produksi pasangan, namun hanya terjadi dengan keberadaan partikel bermuatan di dekatnya, seperti inti atom.[93][94]
[sunting] Atom dan molekul

Animasi yang menunjukkan bagaimana dua atom oksigen berinteraksi membentuk molekul oksigen (O2). Awan merah yang berpendar mewakili orbital elektron tiap-tiap atom. Orbital atom 2s dan 2p atom oksigen awal dapat terlihat bergabung menjadi orbital sigma dan orbital pi, menjadikan atom terikat bersama. Orbital 1s tidak bergabung dan dapat terlihat sebagai dua bulatan kecil yang terpisah
Elektron dapat berpindah dari satu orbtial ke orbital lainnya melalui emisi ataupun absorpsi foton yang energinya sesuai dengan perbedaan potensial antar orbital.[95] Metode perpindahan orbital lainnya meliputi pertumbukan dengan partikel elektron lain dan efek Auger.[96] Agar dapat melepaskan diri dari atom, energi elektron haruslah ditingkatkan melebihi energi pengikatannya. Ini terjadi pada efek fotolistrik, di mana foton yang berenergi lebih tinggi dari energi ionisasi atom diserap oleh elektron.[97]
Momentum sudut orbital elektron terkuantisasi. Oleh karena elektron bermuatan, ia menghasilkan momen magnetik orbital yang proposional terhadap momentum sudut. Keseluruhan momen magnetik sebuah atom adalah setera dengan jumlah vektor momen magnetik orbital dan momen magnetik spin keseluruhan elektron dan inti atom. Namun, momen magnetik inti sangatlah kecil dan dapat diabaikan jika dibandingkan dengan elektron. Momen magnetik dari dua elektron yang menduduki orbital yang sama (disebut elektron berpasangan) akan saling meniadakan.[98]
Ikatan kimia antaratom terjadi sebagai akibat dari interaksi elektromagnetik, sebagaimana yang dijelaskan oleh hukum mekanika kuantum.[99] Ikatan yang terkuat terbentuk melalui perkongsian elektron maupun transfer elektron di antara atom-atom, mengizinkan terbentuknya molekul.[8] Dalam molekul, pegerakan elektron dipengaruhi oleh beberapa inti atom dan elektron menduduki orbital molekul, sama halnya dengan elektron yang menduduki orbital atom pada atom bebas.[100] Faktor mendasar pada struktur molekul adalah keberadaan pasangan elektron. Kedua elektron yang berpasangan memiliki spin yang berlawanan, mengizinkan keduanya menduduki orbital molekul yang sama tanpa melanggar asas pengecualian Pauli. Orbital-orbital molekul yang berbeda memiliki distribusi spasial rapatan elektron yang berbeda pula. Sebagai contohnya, pada elektron berpasangan yang terlibat dalam ikatan, elektron dapat ditemukan dengan probabilitas yang tinggi disekitar daerah inti atom tertentu yang sempit, manakala pada elektron berpasangan yang tidak terlibat dalam ikatan, ia dapat terdistribusi pada ruang yang luas di sekitar inti atom.[101]
[sunting] Konduktivitas
Jika sebuah benda memiliki elektron yang berlebih atau kurang dari yang diperlukan untuk menyeimbangkan muatan inti atom yang positif, benda tersebut akan memiliki muatan listrik. Ketika terdapat elektron berlebih, benda tersebut dikatakan bermuatan negatif. Apabila terdapat elektron yang kurang dari jumlah proton dalam inti atom, benda tersebut dikatakan bermuatan positif. Ketika jumlah elektron dan jumlah proton adalah sama, muatan keduanya meniadakan satu sama lainnya dan benda tersebut dikatakan bermuatan netral. Benda makro dapat menjadi bermuatan listrik melalui penggosokan dan menghasilkan efek tribolistrik.[105]
Elektron tunggal yang bergerak dalam vakum diistilahkan sebagai elektron bebas. Elektron-elektron dalam logam juga berperilaku seolah-olah bebas. Dalam kenyataannya, partikel yang umumnya diistilahkan elektron dalam logam dan padatan lainnya merupakan kuasi-elektron-kuasi-partikel, yang memiliki muatan listrik, spin, dan momen magnetik yang sama dengan elektron asli, namun bermassa berbeda.[106] Ketika elektron bebas bergerak dalam vakum ataupun dalam logam, ia akan menghasilkan aliran muatan yang disebut sebagai arus listrik. Arus listrik ini kemudian akan menghasilkan medan magnetik. Sebaliknya, arus dapat diciptakan pula dengan mengubah medan magnetik. Interaksi ini dinyatakan secara matematis menggunakan persamaan Maxwell.[107]
Pada suhu tertentu, tiap-tiap material memiliki konduktivitas listrik yang menentukan nilai arus listriknya ketika potensial listrik dialirkan kepadanya. Contoh benda yang memiliki konduktivitas listrik yang baik (disebut konduktor) misalnya emas dan tembaga, sedangkan gelas dan teflon adalah konduktor yang buruk. Dalam material dielektrik, elektron tetap terikat pada atom penyusunnya dan material tersebut berperilaku seperti insulator. Sebaiknya logam memiliki struktur pita elektronik yang mengandung pita elektronik yang terisi sebagian. Keberadaan pita tersebut mengizinkan elektron dalam logam berperilaku seolah-olah bebas (elektron terdelokalisasi). Elektron yang terdelokalisasi ini tidak terikat pada atom apapun, sehingga ketika dialiri medan listrik, elektron tersebut akan bergerak bebas seperti gas (gas fermi)[108] melalui material tersebut seperti elektron bebas.
Oleh karena tumbukan antara elektron dengan atom, kecepatan hanyatan elektron dalam konduktor memiliki kisaran milimeter per detik. Namun, kecepatan rambatan elektron biasanya adalah sekitar 75% kecepatan cahaya.[109] This occurs because electrical signals propagate as a wave, with the velocity dependent on the dielectric constant of the material.[110]
Logam merupakan konduktor panas yang baik, utamanya disebabkan oleh elektron terdelokalisasi yang bebas untuk mentranspor energi termal antaratom. Namun, berbeda dengan konduktivitas listrik, konduktivitas termal logam hampir tidak tergantung pada suhu. Konduktivitas termal diekspresikan secara matematis menurut hukum Wiedemann-Franz,[108] yang menyatakan bahwa rasio konduktivitas termal terhadap konduktivitas listrik berbanding lurus terhadap temperatur. Kebalauan termal dalam kisi logam meningkatkan resistivitas listrik material, sehingganya membuat arus listrik tergantung pada temperatur.[111]
Ketika didinginkan di bawah temperatur kritis, material dapat mengalami transisi fase yang menyebabkannya kehilangan semua resistivitas arus listrik. Hal ini dinamakan superkonduktivitas. Dalam teori BCS, perilaku ini dimodelkan oleh pasangan elektron yang memasuki keadaan kuantum kondensat Bose-Einstein. Pasangan Cooper ini memiliki gerakan yang dikopling oleh materi sekitar via getaran kekisi yang disebut fonon, sehingga elektron dapat menghindari tumbukan dengan atom-atom material yang menciptakan hambatan listrik.[112] (Pasangan Cooper memiliki jari-jari sekitar 100 nm, sehingga dapat bertumpang tindih satu sama lain.)[113] Walaupun begitu, mekanisme mengenai bagaimana superkonduktor temperatur tinggi bekerja masih belumlah terpecahkan.
Elektron yang berada dalam padatan konduktor, yang sendirinya juga merupakan kuasipartikel, ketika dikungkung secara ketat pada temperatur yang mendekati nol absolut, akan berperilaku seolah-olah terbelah lebih jauh menjadi dua kuasipartikel: spinon dan holon.[114][115] Spinon memiliki spin dan momen magnetik, sedangkan holon memiliki muatan listrik.
[sunting] Gerak dan energi
Menurut teori relativitas khusus Einstein, seiring dengan bertambahnya kecepatan elektron mendekati kecepatan cahaya, massa relativitas elektron akan meningkat menurut pemantau, sehingga membuatnya semakin sulit mempercepat diri dari kerangka acuan pemantau. Kecepatan elektron dapat mendekati, tetapi tidak dapat mencapai, kecepatan cahaya dalam vakum senilai c. Namun, ketika elektron yang bergerak mendekati kecepatan cahaya c dimasukkan ke dalam media dielektrik seperti air, kecepatan cahaya lokal secara signifikan kurang dari c, sehingganya elektron bergerak melebihi kecepatan cahaya dalam medium tersebut. Ketika elektron berinteraksi dengan medium tersebut, interaksi ini akan menghasilkan pendaran cahaya yang dinamakan radiasi Cherenkov.[116]Efek relativitas khusus ini didasarkan pada faktor Lorentz, didefinisikan sebagai
 dengan v adalah kecepatan partikel. Energi kinetik Ke sebuah elektron yang bergerak dengan kecepatan v adalah:
dengan v adalah kecepatan partikel. Energi kinetik Ke sebuah elektron yang bergerak dengan kecepatan v adalah:Oleh karena elektron dapat berperilaku seperti gelombang, ia akan memiliki karakteristik panjang gelombang de Broglie. Nilai ini adalah λe = h/p dengan h adalah konstanta Planck dan p adalah momentum.[42] Untuk 51 GeV elektron di atas, panjang gelombangnya adalah sekitar 2,4 × 10-17 m. Nilai ini cukup kecil untuk menjelajahi struktur yang lebih kecil dari inti atom.[118]
[sunting] Pembentukan
Teori Big Bang merupakan teori ilmiah yang paling luas diterima sebagai penjelasan atas berbagai tahapan awal evolusi alam semesta.[119] Beberapa milidetik setelah Big Bang, temperatur alam semesta lebih dari 10 milyar kelvin dan foton memiliki energi rata-rata lebih dari satu juta elektronvolt. Foton ini memiliki energi yang cukup sehingganya dapat bereaksi satu sama lainnya membentuk pasangan elektron dan positron,
Semasa proses leptogenesis, terdapat jumlah elektron yang lebih banyak daripada positron. Sampai sekarang, masihlah belum jelas mengapa elektron dapat berjumlah lebih banyak daripada positron.[121] Sekitar satu dari satu milyar elektron lolos dari proses pemusnahan. Kelebihan jumlah proton dibandingkan antiproton juga terjadi dalam kondisi asimetri barion, menyebabkan muatan total alam semesta menjadi nol.[122][123] Proton dan neutron yang tidak musnah kemudian mulai berpartisipasi dalam reaksi nukleosintesis, membentuk isotop hidrogen dan helium, serta sekelumit litium. Proses ini mencapai puncaknya setelah lima menit.[124] Neutron yang tersisa kemudian menjalani peluruhan beta negatif dengan umur paruh sekitar seribu detik, melepaskan proton dan elektron dalam prosesnya,
Kira-kira satu juta tahun setelah big bang, generasi bintang pertama mulai terbentuk.[126] Dalam bintang, nukleosintesis bintang mengakibatkan pembentukan positron dari penggabungan inti atom. Partikel antimateri ini dengan segera memusnahkan elektron dan melepaskan sinar gama. Oleh sebab itu, terjadi penurunan jumlah elektron yang diikuti dengan peningkatan jumlah neutron dengan kuantitas yang sama. Walau demikian, proses evolusi bintang dapat pula mengakibatkan sintesis isotop-isotop radioaktif. Beberapa isotop tersebut kemudian dapat menjalani peluruhan beta negatif dan memancarkan elektron dan antineutrino dari inti atom.[127] Salah satu contohnya adalah isotop kobalt-60 (60Co) yang meluruh menjadi nikel-60 (60Ni).[128]
Pada akhir masa kehidupannya, bintang yang bermassa lebih dari 20 massa surya dapat menjalani keruntuhan gravitasi dan membentuk lubang hitam.[129] Menurut fisika klasik, objek luar angkasa yang sangat berat ini menghasilkan gaya tarik gravitasi yang sangat besar sehingganya tiada benda apapun, termasuk radiasi elektromagnetik, yang dapat lolos dari jari-jari Schwarzschild. Namun, dipercayai bahwa efek mekanika kuantum mengizinkan radiasi Hawking dipancarkan pada jarak ini. Elektron (dan positron) diperkirakan diciptakan di horizon persitiwa lubang hitam.
Ketika pasangan-pasangan partikel maya (seperti elektron dan positron) tercipta disekitar horizon peristiwa, distribusi spasial acak partikel-partikel ini mengizinkan salah satu partikel muncul pada bagian eksterior; proses ini disebut sebagai penerowongan kuantum. Potensial gravitasi lubang hitam kemudian dapat memasok energi yang mengubah partikel maya menjadi partikel nyata, mengizinkannya beradiasi keluar menuju luar angkasa.[130] Sebagai gantinya, pasangan lainnya akan mendapatkan energi negatif, yang menyebabkan penurunan massa-energi lubang hitam. Laju radiasi Hawking meningkat seiring dengan menurunnya massa, pada akhirnya akan menyebabkan lubang hitam "menguap" sampai akhirnya meledak.[131]
Sinar kosmis adalah partikel-partikel yang bergerak di luar angkasa dengan energi yang tinggi. Energi sebesar 3,0 × 1020 eV telah tercatat.[132] Ketika partikel-partikel ini bertumbukan dengan nukleon di atmosfer Bumi, hujanan partikel-partikel dihasilkan, termasuk pula pion.[133] Lebih dari setengah radiasi kosmis yang terpantau dari permukaan Bumi terdiri dari muon. Partikel ini merupakan sejenis lepton yang dihasilkan di atmosfer bagian atas melalui peluruhan pion. Muon, pada gilirannya, dapat meluruh menjadi elektron maupun positron. Oleh karena itu, untuk pion bermuatan negatif π−,[134]
[sunting] Pengamatan
Pengamatan elektron dari jauh memerlukan alat yang mampu mendeteksi energi radiasi elektron tersebut. Sebagai contohnya, dalam lingkungan berenergi tinggi seperti korona bintang, elektron bebas yang berbentuk plasma meradiasikan energinya oleh karena Bremsstrahlung. Gas elektron dapat menjalani osilasi plasma, yang merupakan gelombang yang disebabkan oleh variasi pada rapatan elektron yang sinkron. Hal ini kemudian menghasilkan emisi energi yang dapat dideteksi menggunakan teleskop radio.[136]Frekuensi sebuah foton berbanding lurus dengan energinya. Elektron yang terikat pada inti atom dengan aras energi tertentu akan menyerap ataupun memancarkan foton pada frekuensi aras energi tersebut. Contohnya, ketika atom diiradiasi oleh sumber energi berspektrum lebar, garis-garis absorpsi tertentu akan muncul pada spektrum radiasi yang ditransmisikan. Tiap-tiap unsur ataupun molekul yang berbeda akan menampakkan garis-garis spektrum yang berbeda-beda pula. Pengukuran spektroskopi terhadap kekuatan dan lebar garis-garis spektrum ini memungkinkan penentuan komposisi kimia dan sifat fisika suatu zat.[137][138]
Dalam laboratorium, interaksi elektron individu dapat dipantau menggunakan detektor partikel, yang memungkinkan pengukuran sifat-sifat fisika elektron seperti energi, spin, dan muatannya.[97] Dikembangkannya perangkap Paul dan perangkap Penning mengizinkan partikel bermuatan diperangkap ke dalam suatu daerah tertentu untuk masa yang lama. Hal ini mengizinkan pengukuran yang cermat mengenai sifat dan ciri partikel. Dalam satu percobaan, perangkap Penning dapat memerangkap satu elektron tunggal dalam periode waktu 10 bulan.[139] Momen magnetik elektron yang telah diukur, telah mencapai presisi pengukuran hingga 11 digit. Pada saat itu (1980), pengukuran ini lebih akurat daripada pengukuran konstanta fisika lainnya.[140]
Gambar video pertama yang memperlihatkan distribusi energi elektron direkam oleh sekelompok ilmuwan di Universitas Lund Swedia pada Februari 2008. Para ilmuwan ini menggunakan kilatan cahaya yang sangat pendek, disebut sebagai pulsa attosekon (10-18), mengizinkan gerak elektron dipantau untuk pertama kalinya.[141][142]
Distribusi elektron dalam material padat dapat divisualisasikan menggunakan ARPES (angle resolved photoemission spectroscopy). Teknik ini menggunakan efek fotolistrik untuk mengukur ruang timbal-balik, yaitu suatu representasi struktur periodik yang digunakan untuk menduga struktur awal material. ARPES dapat digunakan untuk menentukan arah, kecepatan, dan sebaran elektron dalam material.[143]
[sunting] Aplikasi
[sunting] Berkas partikel

Semasa uji terowongan angin NASA, sebuah model Pesawat ulang-alik ditembakkan hujan elektron untuk mensimulasikan efek gas pengion sewaktu memasuki bumi.[144]
Litografi berkas elektron (EBL) merupakan suatu metode pengetsaan semikonduktor dengan resolusi lebih kecil dari satu mikron.[148] Teknik ini berbiaya tinggi, lambat, dan perlu dioperasikan secara vakum dan cenderung mengakibatkan sebaran elektron pada padatan. Oleh karena sebaran ini, resolusinya terbatas pada 10 nm. Oleh karenanya, EBL utamanya digunakan pada produksi sejumlah kecil sirkuit terpadu yang terspesialisasi.[149]
Pemrosesan berkas elektron digunakan untuk mengiradiasi material agar sifat-sifat fisikanya berubah ataupun untuk tujuan sterilisasi produk makanan dan medis.[150] Dalam terapi radiasi berkas elektron dihasilkan oleh pemercepat liner untuk pengobatan tumor superfisial. Oleh karena berkas elektron hanya menembus kedalaman yang terbatas sebelum diserap, biasanya sampai dengan 5 cm untuk elektron berenergi 5–20 MeV, terapi elektron berguna untuk mengobati lesi kulit seperti karsinoma sel basal. Berkas elektron dapat digunakan untuk mensuplemen perawatan daerah-daerah yang telah diiradiasi oleh sinar-X.[151][152]
Pemercepat partikel menggunakan medan listrik untuk membelokkan elektron dan antipartikelnya mencapai energi tinggi. Oleh karena partikel ini bergerak melalui medan magnetik, ia memancarkan radiasi sinkrotron. Intensitas radiasi ini bergantung pada spin, yang menyebabkan polarisasi berkas elektron (dikenal sebagai efek Sokolov-Ternov). Berkas elektron yang terpolarisasi ini dapat digunakan dalam berbagai eksperimen. Radiasi sinkotron juga dapat digunakan untuk pendinginan berkas elektron, yang menurunkan sebaran momentum partikel. Seketika partikel telah dipercepat sampai pada energi yang ditentukan, elektron dan positron ditumbukkan. Emisi energi yang dihasilkan oleh tumbukan tersebut dipantau menggunakan detektor partikel dan dipelajari dalam fisika partikel.[153]
[sunting] Pencitraan
Difraksi elektron berenergi rendah (Low-energy electron diffraction) adalah suatu metode penghujanan bahan-bahan kristalin dengan berkas kolimasi elektron untuk kemudian dipantau pola-pola difraksi yang dihasilkan untuk menentukan struktur material tersebut. Energi yang diperlukan pada umumnya berkisar antara 20–200 eV.[154] Difraksi elektron berenergi tinggi refleksi (reflection high energy electron diffraction) adalah teknik yang menggunakan refleksi berkas elektron yang ditembakkan pada berbagai sudut rendah untuk mengkarakterisasikan permukaan material kritsalin. Energi berkas biasanya berkisar antara 8–20 keV dan sudut tembakan adalah 1–4°.[155][156]Mikroskop elektron mengarahkan berkas elektron yang difokuskan kepada suatu spesimen. Pada saat berkas berinteraksi dengan spesimen, beberapa elektron berubah sifatnya, misalnya pada arah pergerakan, sudut, energi, dan fase relatif elektron. Dengan mencatat perubahan pada berkas elektron, para ilmuwan dapat menghasilkan citra material yang diperbesar tersebut.[157]
[sunting] Lihat pula
[sunting] Catatan kaki
- ^ Penyebut versi pecahannya merupakan balikan nilai desimal (dengan ketidakpastian standar relatif 4,2 × 10-10).
- ^ Muatan elektron adalah negatif muatan elementer yang memiliki nilai positif untuk proton.
- ^ Besaran ini didapatkan dari bilangan kuantum spin sebagai
Lihat: Gupta, M. C. (2001). Atomic and Molecular Spectroscopy. New Age Publishers. hlm. 81. ISBN 8122413005. - ^ Bohr magneton:
- ^ Jari-jari elektron klasik diturunkan sebagai berikut. Asumsikan bahwa muatan elektron tersebar merata di seluruh volume bola partikel. Oleh karena satu bagian bola tersebut akan menolak bagian yag lainnya, bola tersebut mengandung energi potensial elektrostatik. Energi ini diasumsikan sama dengan energi rihat elektron, yang ditentukan melalui teori relativitas khusus (E=mc2).
Dari teori elektrostatistika, energi potensial suatu bola dengan jari-jari r dan muatan e adalah:
Lihat: Haken, Hermann (2005). The Physics of Atoms and Quanta: Introduction to Experiments and Theory. Springer. hlm. 70. ISBN 3540672745. - ^ Radiasi yang berasal dari elektron non-relativistik kadang-kadang disebut radiasi siklotron.
- ^ Perubahan pada panjang gelombang Δλ bergantung pada sudut pentalan θ sebagai berikut
- ^ Dengan mencari kecepatan elektron dan menggunakan pendekatan untuk nilai γ yang besar, kita akan mendapatkan:




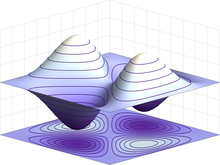


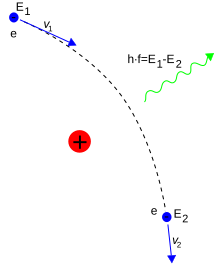
















0 komentar: